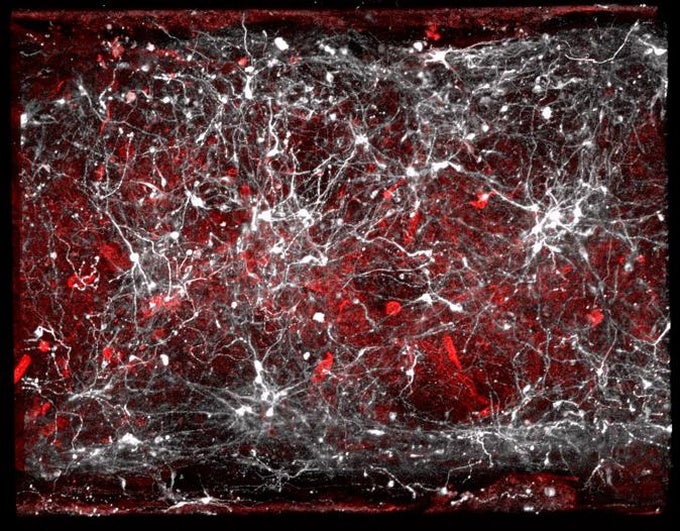
Vieron lo invisible que activa el Parkinson
¡Atención, amantes de la ciencia y la medicina! Tenemos una noticia que está revolucionando la investigación sobre una de las enfermedades neurológicas que más nos preocupa. Por primera vez en la historia, un equipo científico ha logrado visualizar directamente los grupos de proteínas que se cree son los responsables de desencadenar el Párkinson. Esto es un verdadero punto de inflexión en la lucha contra esta enfermedad, que no deja de crecer a un ritmo alarmante a nivel global.
Hasta ahora, estos pequeños grupos, conocidos como oligómeros de alfa-sinucleína, eran como fantasmas. Se les sospechaba de ser los principales culpables en el desarrollo del Párkinson, pero su tamaño diminuto los había mantenido ocultos a la vista en el tejido cerebral humano. ¡Imagina tener un sospechoso clave en un caso gigante, pero sin poder verlo! Pues eso era lo que pasaba. La capacidad de por fin ‘ver’ estos oligómeros nos abre un mundo de posibilidades para entender cómo se propaga la enfermedad y, lo más importante, cómo podemos detenerla.
La Reinvención del Detective Científico: Nace la Técnica ASA-PD
El mérito de este logro colossal va para un grupo de mentes brillantes de la Universidad de Cambridge, la UCL, el Instituto Francis Crick (Reino Unido) y la Politécnica de Montreal (Canadá). Juntos, han desarrollado una técnica de imagen tan sofisticada que nos permite no solo ver, sino también contar y comparar estos oligómeros en el tejido cerebral humano. ¡Es como si hubieran equipado a los científicos con unos superpoderes para ver lo invisible!
Esta técnica se llama ASA-PD (¡apúntenla bien!) y se basa en la microscopía de fluorescencia ultrasensible. ¿Qué significa esto? Pues que dispara la sensibilidad a niveles nunca antes vistos, permitiendo detectar y analizar oligómeros de alfa-sinucleína en cerebros post mortem. Es como afinar el oído para escuchar el susurro más leve en medio de un concierto de rock. Al maximizar la señal y reducir el ruido de fondo, han conseguido un hito increíble: observar y estudiar incluso oligómeros individuales. Esto no es solo un pequeño paso, es un salto gigantesco para la ciencia.
El Párkinson: Un Enemigo que Crece y el Desafío de Detenerlo
Las cifras son claras y preocupantes: para el año 2050, se espera que la cantidad de personas con Párkinson en el mundo se duplique, alcanzando la escalofriante cifra de 25 millones. A pesar de que existen tratamientos que ayudan a mejorar síntomas como el temblor o la rigidez, la triste realidad es que todavía no contamos con fármacos que puedan frenar o detener el avance de la enfermedad. Y ahí radica la urgencia y la importancia de hallazgos como este.
Tradicionalmente, el Párkinson se ha diagnosticado por la presencia de los llamados cuerpos de Lewy, unos grandes depósitos de proteínas que se forman en el cerebro. Sin embargo, los investigadores sospechaban desde hace mucho tiempo que los verdaderos culpables iniciales eran estos oligómeros de alfa-sinucleína, mucho más pequeños y que aparecen en las primeras fases de la enfermedad. El profesor Steven Lee, codirector de esta investigación, lo explica a la perfección: “Los cuerpos de Lewy son la señal de que la enfermedad ya está instaurada, pero no nos dicen cómo empezó”. Según él, poder ver la enfermedad en sus etapas más tempranas es clave para entenderla y, en última instancia, tratarla con eficacia.
Una Ventana al Cerebro Humano: Ver Estrellas a Plena Luz del Día
Rebecca Andrews, una de las autoras principales del estudio, lo describe de una forma muy gráfica: “Es como ver estrellas a plena luz del día”. ¡Imagínense! La analogía es perfecta para entender la magnitud de lo que han logrado. Por primera vez, han podido observar estos oligómeros directamente en tejido cerebral humano y a una escala que era impensable hasta ahora. Este avance abre puertas que antes estaban completamente cerradas en la investigación del Párkinson.
El estudio comparó cerebros post mortem de personas diagnosticadas con Párkinson con los de individuos sanos. Lo que encontraron fue revelador: aunque había oligómeros en ambos casos, en los cerebros con Párkinson estos eran más grandes, más brillantes y mucho más abundantes. Esto sugiere una conexión directa entre estos oligómeros y la progresión de la enfermedad. Además, identificaron una subclase de oligómeros que es exclusiva de los pacientes con Párkinson, lo que podría ser un marcador temprano crucial, incluso antes de que los síntomas se manifiesten.
Un Atlas de Cambios y los Retos que Vienen
Esta innovadora técnica no solo arroja luz sobre el Párkinson, sino que ofrece una especie de “atlas” de cambios proteicos que podría ser útil en el estudio de otras enfermedades neurodegenerativas. Podría ayudarnos a identificar qué tipos específicos de células se ven afectadas, acercándonos a tratamientos más precisos. Los investigadores insisten en que estudiar directamente el cerebro humano es fundamental, aunque sabemos que es un camino complejo. La tecnología ASA-PD es un faro que ilumina nuevas vías para entender cómo estos agregados proteicos perturban el entorno cerebral y disparan la enfermedad.
Sin embargo, el camino no está exento de desafíos. Salvador Ventura, director científico del Instituto de Investigación e Innovación Parc Taulí, advierte que, aunque la técnica es un gran avance, hay que ser cautos con la definición de “oligómero”. Pueden abarcar una variedad de estructuras en diferentes etapas de la enfermedad. Podrían ser, dice, “pequeños agregados prefibrilares” más grandes que los oligómeros tóxicos descritos en otros estudios. Pero que no haya dudas: el hallazgo es importantísimo porque logra detectar estas especies sin necesidad de amplificación indirecta, lo que lo hace mucho más directo y revelador.
El gran reto ahora es llevar esta técnica del laboratorio a la clínica. Esto implica superar obstáculos técnicos y regulatorios, como aumentar la sensibilidad para poder aplicarla en tejidos vivos y desarrollar marcadores seguros que permitan un diagnóstico temprano. La combinación de un diagnóstico precoz con terapias que puedan modificar el curso de la enfermedad sería el escenario ideal, y la técnica ASA-PD tiene el potencial de ser una pieza clave en este rompecabezas. ¡En Vinyl Station Radio seguiremos de cerca estos avances que nos tienen a todos en vilo!
Fuente original de la información: ABC – R. Ibarra
Créditos de la imagen: NIH